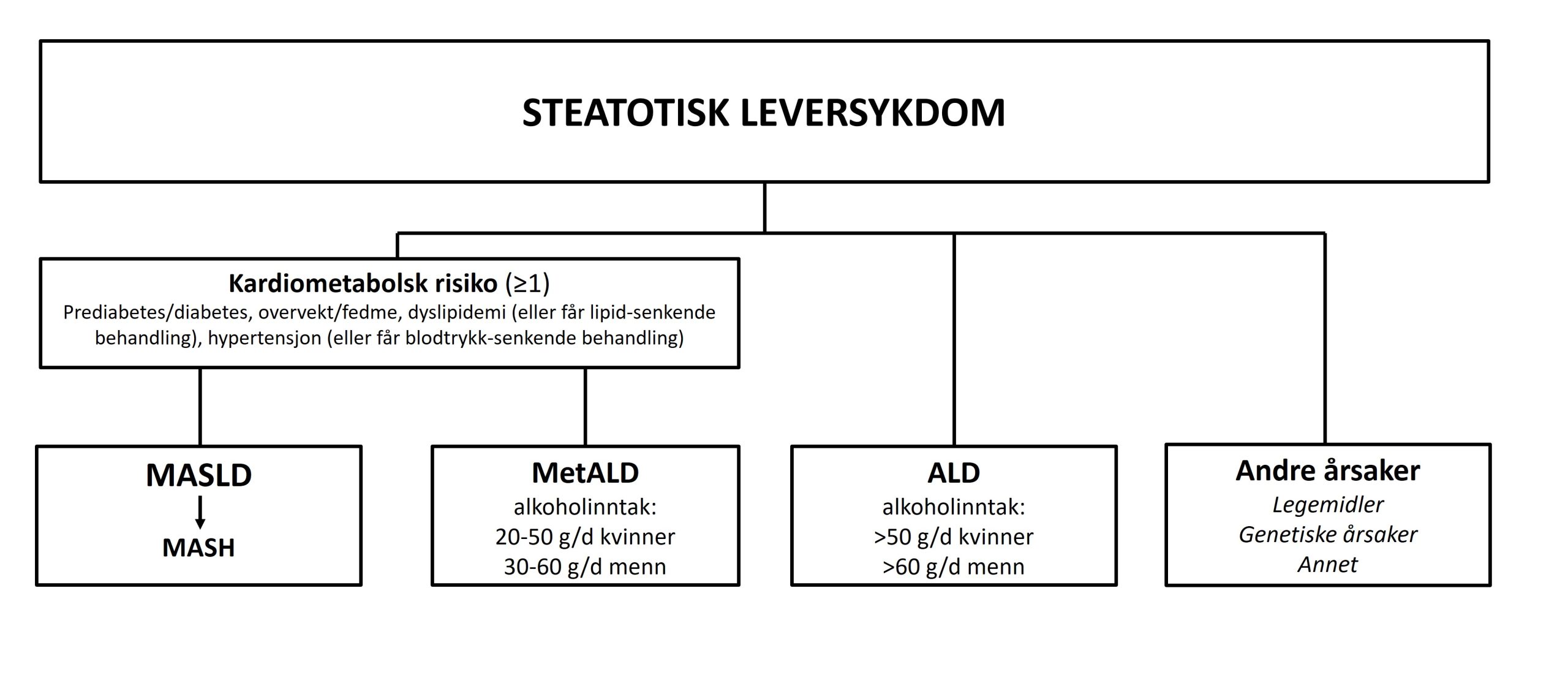
Inndeling av steatotisk leversykdom basert på kardiometabolsk risiko, alkoholoverforbruk og alternative årsaker til steatose. Ved kardiometabolsk risiko (overvekt/fedme, type 2-diabetes, hypertensjon, dyslipidemi) klassifiseres steatose som MASLD ved alkoholforbruk under terskler for MetALD/ALD; ved inflammasjon og hepatocytt-ballooning på biopsi betegnes tilstanden som MASH. MetALD defineres ved kardiometabolsk risiko i kombinasjon med alkoholforbruk 20-50 g/dag hos kvinner og 30-60 g/dag hos menn. ALD defineres ved alkoholforbruk >50 g/dag hos kvinner og >60 g/dag hos menn. Andre årsaker til steatose (inkludert DILI/DISH, monogene og sekundære årsaker) vurderes parallelt; dersom ingen årsak identifiseres, klassifiseres tilstanden som ukjent årsak (kryptogen).
utreDning og behandling
Omfang, målgruppe og prinsipper
Innholdet er rettet mot sykehusspesialister (gastroenterologi, indremedisin, radiologi og laboratoriemedisin). Fokus er MASLD/MASH og ALD, men prinsipper for triagering, ikke-invasive tester (NIT) og oppfølging gjelder bredt. Hovedmål: tidlig risikostratifisering, standardisert bruk av NIT, korrekt håndtering av feilkilder og sømløse henvisningsløp.
Diagnostikk – spesialistnivå
Pasienter henvises typisk etter positiv førstelinjescreening i primærhelsetjenesten (FIB-4 ≥ aldersspesifikk terskel) og/eller ved klinisk mistanke om avansert fibrose. På spesialistnivå kombineres ELF og/eller leverstivhetsmåling (LSM) med klinikk, laboratorier og etiologisk avklaring.
Ikke-invasive tester (NIT)
- ELF (andrelinje etter positiv FIB-4 hos voksne ≥ 35 år): tolkes mot veilederens beslutningsgrenser (typisk < 9,8 lav risiko; ≥ 9,8 moderat/høy). Unngås ved akutt alkoholisk hepatitt og «varm fase».
- LSM (VCTE/FibroScan eller ultralyd-elastografi/SWE):
- < 8 kPa: lav sannsynlighet for avansert fibrose; kontroll i primærhelse ved stabil klinikk.
- 8–15 kPa: gråsone; repeter LSM i «kald fase» og/eller suppler med ELF; vurder etiologi og komorbiditet.
- > 15 kPa: sannsynlig avansert fibrose/cirrhose; plan for spesialistoppfølging.
- MR-elastografi (MRE) vurderes ved motstridende funn eller tekniske begrensninger (fedme, ascites, artefakter), og gir presis staging der tilgjengelig.
Vanlige feilkilder/konfoundere
- LSM: inflammasjon, kolestase, hjertesvikt, nylig alkoholinntak, høy BMI, postprandial status; repetering i «kald fase» reduserer falsk forhøyede verdier. Ascites kan gjøre VCTE ikke-målbart → vurder SWE/MRE.
- ELF: kan være forhøyet ved akutt leverskade og i andre fibrotiske tilstander (f.eks. lungefibrose) og ved leverstuvning.
- FIB-4: ikke validert < 35 år; påvirkes ved hematologiske avvik (trombocytter), pågående inflammasjon/avrusning/akutt alkoholisk hepatitt.
Etiologisk avklaring – nødvendig standardpanel
Bekreft og kvantitér alkoholbruk (AUDIT-C, PEth), kartlegg kardiometabolske risikofaktorer (T2D, dyslipidemi, hypertensjon), og utelukk øvrige leveretiologier (HBsAg, anti-HBc, anti-HCV/HCV-RNA; ferritin/transferrinmetning; autoantistoffer og IgG ved autoimmun hepatitt; ALP/GGT/AMA ved kolestase/PSC/PBC; vurder A1AT-mangel/Wilson ved klinisk mistanke). Billeddiagnostikk (UL og ev. MR) ved avvikende leverprøver, palpasjonsfunn, eller ved plan for HCC-screening.
Portal hypertensjon og varicescreening
Følg Baveno VII for ikke-invasiv prediksjon av klinisk signifikant portal hypertensjon (CSPH) og for å redusere unødvendig gastroskopi. Kombinasjon av LSM og trombocytter kan identifisere pasienter som trygt kan avstå fra primær varicescreening, og de som trenger endoskopi og primærprofylakse.
Prinsipp: lav LSM + normale/lett reduserte trombocytter → lav CSPH-sannsynlighet; høy LSM ± trombocytopeni → økt CSPH-sannsynlighet og behov for gastroskopi.
Alkoholrelatert leversykdom (ALD)
Ved mistenkt/alvorlig alkoholisk hepatitt bruk Maddrey DF for risikostratifisering; vurder Lille score under behandling dersom aktuelt. Ved stabil ALD følges NIT-løp analogt til MASLD (ELF/LSM) med oppfølging av komorbiditeter, ernæring, og systematiske tiltak for alkoholreduksjon/abstinens. Rekompensering (Baveno VII-kriterier) gir betydelig prognostisk gevinst; vurder revurdering av varice-/HCC-opplegg når kriterier oppnås.
Oppfølging ved avansert fibrose/cirrhose
- Komplikasjoner: ascites (saltrestriksjon, diuretika, albumin ved LVP), HE (laktulose ± rifaksimin), varicer (NSBB og/eller ligering etter retningslinjer), HRS-AKI (albumin + vasokonstriktor; transplantasjonsvurdering).
- HCC-overvåkning: UL (med/uten AFP) hver 6. måned hos pasienter med cirrhose, uavhengig av etiologi; følg standard opptrapping til kontrast-CT/MR ved SUS-funn.
- Vaksinasjon og forebygging: HBV, HAV ved ikke-immun status; osteoporoseprofylakse etter behov.
- Transplantasjonsvurdering: MELD-Na som grunnlag for prioritering; vurder TIPS i utvalgte portalhypertensjons-scenarier etter gjeldende konsensus.
MASLD/MASH – behandlingsrammer
Intervensjoner inkluderer målrettet vektreduksjon (5–10 % for bedring av steatose/nekroinflammasjon/fibrose), strukturert fysisk aktivitet, optimalisering av glykemisk kontroll, blodtrykk og lipider, samt tett oppfølging av alkoholbruk. Farmakoterapi ved MASH er i utvikling; anvend gjeldende retningslinjer og legemiddelmyndighetenes føringer.
Kontroll og re-testing
- Lav risiko: re-test med FIB-4/ELF/LSM innen 1–3 år avhengig av risikoprofil og komorbiditet.
- Gråsone: gjenta i «kald fase» (4–12 uker) og supplér med alternativ NIT.
- Høy risiko/avklart cirrhose: strukturert oppfølging (komplikasjonsprofylakse, HCC-screening, ernæring, transplantasjonsvurdering ved behov).
Kliniske verktøy
Bruk lokale kalkulatorer og laboratorierapporter i tråd med veileder. Se også «Kliniske verktøy»-siden på leverfibrose.no for FIB-4, AUDIT-C, MELD-Na, Child–Pugh m.fl.
Referanser
- EASL–EASD–EASO. (2024). Clinical Practice Guidelines on the management of metabolic dysfunction-associated steatotic liver disease (MASLD). Journal of Hepatology. PubMed
- EASL–EASD–EASO. (2024). Clinical Practice Guidelines on the management of MASLD. Obesity Facts, 17(4), 374–444. PubMed
- EASL. (2021). Clinical Practice Guidelines on non-invasive tests for evaluation of liver disease severity and prognosis (update). Journal of Hepatology, 75, 659–689. PubMed
- de Franchis, R., Bosch, J., Garcia-Tsao, G., et al. (2022). Baveno VII – Renewing consensus in portal hypertension. Journal of Hepatology, 76, 959–974. PubMed
- Dietrich, C. F., Bamber, J., Berzigotti, A., et al. (2017). EFSUMB Guidelines on the clinical use of liver ultrasound elastography (short version). Ultraschall Med, 38, 377–394. PubMed
- Barr, R. G., Wilson, S. R., Rubens, D., et al. (2020). Update to the Society of Radiologists in Ultrasound liver elastography consensus statement. Radiology, 296, 263–274. PubMed
- Mózes, F. E., Lee, J. A., Selvaraj, E. A., et al. (2022). Diagnostic accuracy of non-invasive tests for advanced fibrosis in NAFLD: IPD meta-analysis. Gut, 71, 1006–1019. PubMed
- Boursier, J., Hagström, H., Ekstedt, M., et al. (2022). Non-invasive tests accurately stratify NAFLD by risk of liver-related events. Journal of Hepatology, 76, 1013–1020. PubMed
- Xiao, G., Zhu, S., Xiao, X., et al. (2017). Laboratory tests vs ultrasound/MR elastography to detect fibrosis in NAFLD: meta-analysis. Hepatology, 66, 1486–1501. PubMed
- Singal, A. G., Zhang, E., Narasimman, M., et al. (2022). HCC surveillance improves early detection, curative therapy and survival in cirrhosis: meta-analysis. Journal of Hepatology, 77, 128–139. PubMed
- Singal, A. K., & Mathurin, P. (2021). Diagnosis and treatment of alcohol-associated liver disease: A review. JAMA, 326, 165–176. PubMed
- Rasmussen, D. N., Thiele, M., Johansen, S., et al. (2021). Prognostic performance of seven biomarkers vs biopsy in early ALD. Journal of Hepatology, 75, 1017–1025. PubMed
- ElSayed, N. A., Aleppo, G., Aroda, V. R., et al. (2023). ADA Standards of Care 2023: classification & diagnosis (+ addendum). Diabetes Care, 46, S19–S40, S49–S67, 1718–1720. PubMed
- Cusi, K., Isaacs, S., Barb, D., et al. (2022). AACE CPG for NAFLD in primary care & endocrinology (co-sponsored by AASLD). Endocrine Practice, 28, 528–562. PubMed
- GBD 2019 Collaborators. (2020). Global burden of 369 diseases and injuries. The Lancet, 396, 1204–1222. PubMed
- Quek, J., Chan, K. E., Wong, Z. Y., et al. (2023). Global prevalence of NAFLD/NASH in overweight and obese. Lancet Gastroenterol Hepatol, 8, 20–30. PubMed
- Le, M. H., Le, D. M., Baez, T. C., et al. (2023). Global incidence of NAFLD. Journal of Hepatology, 79, 287–295. PubMed
- Dulai, P. S., Singh, S., Patel, J., et al. (2017). Increased mortality risk by fibrosis stage in NAFLD. Hepatology, 65, 1557–1565. PubMed
- Vitale, A., Trapani, S., Russo, F. P., et al. (2024). Waiting list mortality and 5-year transplant survival benefit in MASLD. JHEP Reports, 6, 101147. PubMed

